A leishmaniose é uma doença parasitária endêmica, causada por um protozoário do gênero Leishmania. Ela é transmitida através da picada de insetos, vetores hematófagos, conhecidos como flebotomíneos, pertencentes aos gêneros Lutzomyia, no Novo Mundo, e Phlebotomus, no Velho Mundo. No Brasil, os mosquitos mais comuns, do gênero Lutzomyia, associados à doença são: o “mosquito-palha”, “cangalhinha” e “birigui”. De modo geral, o contágio acontece quando o inseto se contamina com o sangue de pessoas ou animais infectados, podendo, em seguida, transmitir a doença para um hospedeiro saudável.
Durante a picada, o mosquito injeta os promastigotas do protozoário, a forma infectante, dos seus probóscitos (aparelho bucal) para os tecidos. Esses são fagocitados por macrófagos ou outras células do sistema monocítico fagocitário, transformando-se, então, em amastigotas. Na medida em que os amastigotas se multiplicam, os macrófagos se rompem, liberando novos parasitas que serão fagocitados por novas células monocitárias fagocíticas.
Existem mais de 20 espécies de Leishmania que infectam humanos e mais de 70 espécies diferentes de animais que podem ser reservatórios para os parasitas. Nos centros urbanos, por exemplo, os cães e os humanos são os principais hospedeiros. De acordo com a localização geográfica, dois tipos de leishmaniose podem ser encontrados: Novo Mundo e Velho Mundo. Enquanto a forma do Velho Mundo é encontrada no sul da Europa, Oriente Médio, Ásia e África, a forma do Novo Mundo é identificada nas áreas tropicais do México, nas Américas Central e do Sul.
Características Clínicas
Existem três formas clínicas principais de leishmaniose: visceral, cutânea e mucocutânea. A forma visceral é a mais severa e grave, podendo ser fatal em 95% dos casos. Ela é caracterizada por perda de peso, citopenia, hepatoesplenomegalia e, nas Américas, é causada, principalmente, pela L. chagasi. A forma cutânea é a mais comum, mostrando lesões ulceradas com áreas crostosas centrais, com bordas eritematosas bem definidas e localizadas nas áreas do corpo expostas. Os principais agentes causadores são: a L. braziliensis, L. amazonensis, L. guianensis, L. pananmensis e L. mexicana. O período de incubação é de 2 a 4 meses, mas isso pode ser variável. A doença pode levar alguns anos para manifestar-se clinicamente, o que resulta no atraso do diagnóstico.
A leishmaniose mucocutânea é causada principalmente pela L. braziliensis, L. panamensis, e, algumas vezes, pela L. guyanensis e L. amazonensis. Esse tipo é menos frequente e, além da pele, acomete também as mucosas de revestimento do trato respiratório superior, preferencialmente nariz, mas podendo afetar a boca, faringe e laringe. Alguns autores sugerem que a baixa temperatura da cavidade nasal favorece o crescimento do parasita, o que explica porque o septo nasal e a porção anterior da fossa nasal sejam os sítios mais afetados. O envolvimento nasal pode levar a quadro de rinorreia e, eventualmente, perfuração do septo nasal, o que dá origem ao termo clínico de “nariz de tapir”, em razão do edema da mucosa e das estruturas de suporte do nariz (Figura 1). A leishmaniose mucocutânea é endêmica no Brasil, Bolívia, Peru e Etiópia, entre outros países. Pacientes imunossuprimidos são considerados mais suscetíveis à doença. Por isso, devemos ficar atentos para os sinais e sintomas sistêmicos da doença nesse grupo de risco, tais como: febre, calafrio, hepatoesplenomegalia, panticopenia, envolvimento gastrointestinal e ascite.
Em algumas regiões endêmicas, a Leishmaniose de mucosa pode ser primária ou acompanhar, especialmente, a forma cutânea da doença. As lesões podem surgir anos após a regressão das lesões cutâneas e, nesse caso, são resultantes da disseminação hematogênica ou linfática do parasita.
Lesões orais da leishmaniose são raras e podem ser vegetantes, por vezes, eritematosas ou ulceradas, exibindo superfície granular (Figura 2). Elas afetam, especialmente, a mucosa do palato duro e mole. O paciente pode apresentar queixa de disfonia e dificuldade de deglutição. Para o diagnóstico, o clínico deve observar as manifestações clínicas, testes sorológicos, exame microscópico da biópsia, incluindo coloração histológica pelo Giemsa ou exame de imuno-histoquímica para detecção do protozoário. O exame sorológico é mais útil para o diagnóstico da forma visceral, uma vez que apresente valor limitado para as formas cutânea e mucocutânea. O exame de PCR, para pesquisa do protozoário, utilizando material obtido de biópsia, tem grande valor para diagnóstico.
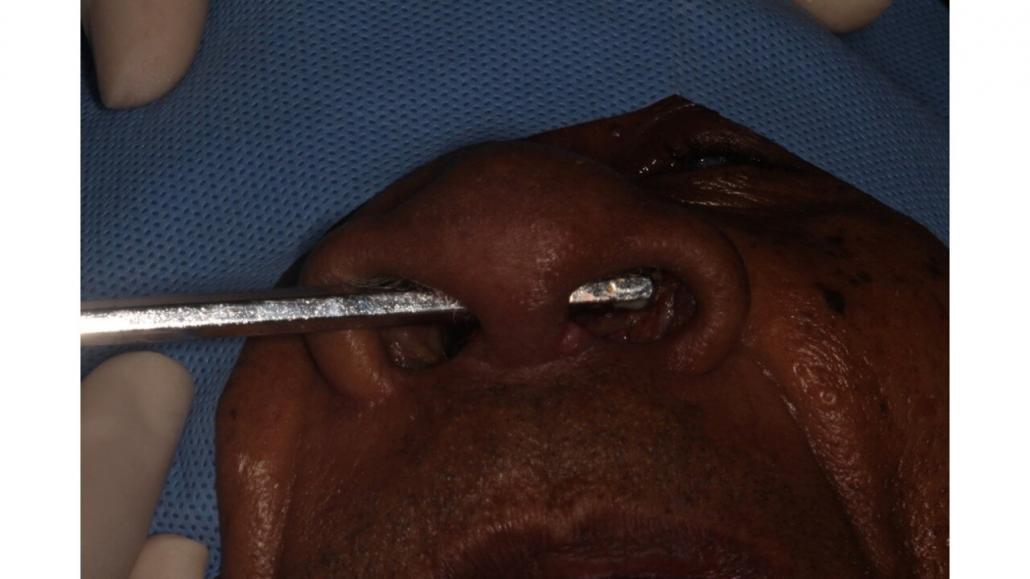
Figura 1- Nariz de tapir e perfuração do septo nasal, características clínicas importante da leishmaniose acometendo a cavidade nasal (Imagem gentilmente cedida pelo Prof. Hélder Pontes).

Figura 2- Manifestação oral da leishmaniose. Observar a aparência vegetante da lesão no palato.
Características histopatológicas
O exame microscópico da leishmaniose mostra inflamação granulomatosa, não necrosada, e de localização subepitelial. O epitélio pode exibir hiperplasia pseudoepiteliomatosa (Figura 3). A presença de macrófagos repletos de amastigotas intracitoplasmáticos, de morfologia arredondada, sugere leishmaniose (Figura 4). Entretanto, o diagnóstico diferencial com histoplasmose deve ser feito. Para isso, três colorações especiais são necessárias: Grocott, PAS e Giemsa. Na leishmaniose, apenas a coloração pelo Giemsa mostrará positividade para as inclusões sugestivas de amastigotas de leishmania (Figura 5). Embora a identificação de cinetoplastos, estruturas intracitoplasmáticas em forma de bastão, no interior de macrófagos, possa ajudar no diagnóstico, estes nem sempre são identificados em cortes histopatológicos (Figura 6). Cabe mencionar que o cinetoplasto é uma rede de DNA circular presente na mitocôndria de alguns protozoários, como leishmaniose e doença de Chagas.
Não é incomum encontrarmos lesões com escassa presença de parasitas. Nesses casos, o exame de PCR, conforme mencionado acima, poderá ajudar.

Figura 3- Corte microscópico em menor aumento de um caso de leishmaniose. Observar hiperplasia pseudoepiteliomatosa e infiltrado crônico subepitelial.

Figura 4- Numerosos macrófagos contendo estruturas arredondadas intracitoplasmáticas (seta), sugestivas de leishmaniose.
 Figura 5- Amastigotas de leishmania corados pelo Giemsa.
Figura 5- Amastigotas de leishmania corados pelo Giemsa.

Figura 6- Pequenas estruturas em bastão, denominadas cinetoplastos (seta), são encontradas em amastigotas e auxiliam no diagnóstico de leishmaniose.
Tratamento
O tratamento da leishmaniose visceral pode ser realizado com anfotericina B lipossomal, meglumina ou pentamida. A escolha da medicação deve ser feita por um médico infectologista, levando em conta uma série de aspectos, incluindo a forma e o quadro clínico do paciente.
Leitura Complementar
1- Botelho MCB, Ferreira LL, Fikaris S, Prado-Ribeiro AC, Soubhia AMP, Biasoli ER, et al. Tongue nodule as primary manifestation of american cutaneous leishmaniasis in an immunocompetent patient. Head Neck Pathol 2021;15:1069-1073.
2- Lessa MM, Lessa HA, Castro TWN, Oliveriva A, Scherifer A, Machado P, et al. Mucosal leishmaniasis: epidemiological and clinical aspects. Rev Bras Otorrinolingol 2007;73:843-847.
3- Mignona MD, Celentano A, Leuci S, Cascone M, Adamo D, Ruoppo E, et al. Mucosal leishmaniasis with primary oral involvement: a case series and a review of the literature. Oral Dis 2015;21:e70-e78.
4- Motta ACF, Lopes MA, Ito FA, Carlos-Breni R, Almeida OP, Roselino AM. Oral leishmaniasis: A pilot clinopathological study of 11 cases. Oral Dis 2007;355-340.
5- Silveira HA, Panucci BZM, Silva EV, Mesquita ATM, León JE. Microscopical diagnosis of oral leishmaniasis: kinetoplast. Head Neck Pathol 2021;15:1085-1086.
Conheça nossos cursos
